Mots clés : Bionum, Brèves, MEG
Etiquettes: ACTH, Cancer, Cellules non endocrines, Hormone, Neurochirurgie, Sciences de la vie, Syndrome de Cushing
Connaissez-vous le syndrome de Cushing ? Ce syndrome découvert le siècle dernier, fut nommé d’après Harvey Cushing, célèbre médecin considéré comme le “Père de la neurochirurgie moderne” ! 100 ans après, les conditions d’apparition de cette maladie restent toujours mal comprises. Anto Krinus nous explique ce mystère !
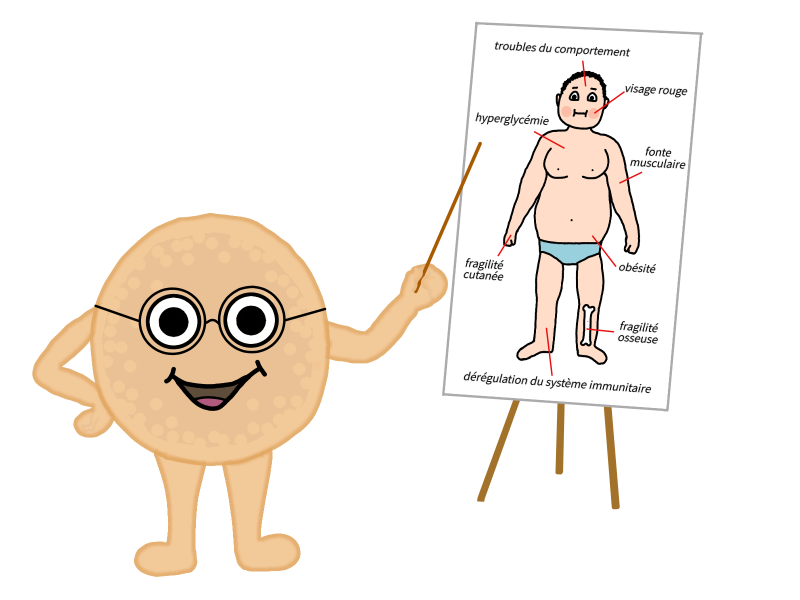
Bonjour à tous, je suis Anto Krinus, laissez-moi vous dire quelques mots sur le syndrome de Cushing. Il est induit par une surproduction de cortisol et est caractérisé par plusieurs symptômes : fragilité osseuse, obésité, trouble du comportement, hyperglycémie, dérégulation du système immunitaire, fonte musculaire, fragilité cutanée et bien d’autres encore.
Vous vous demandez sûrement comment je sais tout cela. Et bien, je suis une cellule endocrine, c’est à dire que je travaille en tant que producteur d’hormone. Mon usine est localisée dans une des glandes surrénales, juste au-dessus des reins. Mes collègues et moi sommes chargés de produire des hormones, des petites molécules que nous envoyons comme signaux dans tout le corps. Je suis personnellement spécialisé dans la production de cortisol, l’hormone du stress. Bien sûr, je ne le fais que quand j’en reçois l’ordre de mes supérieurs, d’autres cellules endocrines qui vivent dans le cerveau. Ils m’en donnent le signal en m’envoyant une hormone avec un nom vraiment affreux : adrénocorticotrophine. On préfère l’appeler ACTH, c’est plus court !
En temps normal, le cortisol permet d’augmenter le taux de sucre dans le sang ou encore de réduire la réponse immunitaire. Mais il arrive que mes supérieurs déraillent complètement et deviennent cancéreux. A ce moment-là, ils se mettent à produire plus de signaux que la normale et nous envoient un surplus d’ACTH. On est donc contraint d’augmenter la production de cortisol sous les ordres de ces supérieurs devenus fous. Au bout du compte, on se retrouve avec un excès de cortisol qui induit le syndrome de Cushing. Je ne vous raconte pas les dégâts pour le corps.
Mais dernièrement, on a découvert que des cellules pouvaient usurper la fonction de nos supérieurs, en produisant de l’ACTH.
On a pu retrouver, chez certains patients atteints du Syndrome de Cushing, des cellules cancéreuses non endocrines, et pourtant capables de produire de l’ACTH. Ces cellules ne ressemblent en rien à mes supérieurs dans le cerveau, elles n’ont initialement pas le même métier et peuvent venir d’un peu n’importe où dans le corps. Elles se mettent à produire l’ACTH en grandes quantités, et le résultat est le même : nous surproduisons le cortisol, ce qui provoque l’apparition du syndrome de Cushing.
Pour comprendre comment ces cellules non endocrines acquièrent cette nouvelle identité, les scientifiques étudient leur ADN, à la recherche de potentielles modifications qui pourraient expliquer comment elles parviennent à produire l’ACTH. La compréhension de l’apparition de cette maladie permettra de mieux caractériser le syndrome de Cushing et ainsi, on l’espère, d’apporter un meilleur traitement aux patients atteints de cette forme du syndrome.
Remerciements
Ce billet de blog a été écrit à la suite d’un stage de Master réalisé sous la direction du Dr Alexandre Buffet au sein de l’équipe 13 “Génétique et Métabolisme des cancers rares” dirigée par Dr Judith Favier et Pr Anne-Paule Gimenez-Roqueplo, Centre de Recherche Cardiovasculaire Paris, INSERM U970.
Bibliographie
Ballav, Chitrabhanu, et al. « Mini-Review: Pheochromocytomas Causing the Ectopic ACTH Syndrome ». Endocrine, vol. 42, no 1, août 2012, p. 69‑73. DOI.org (Crossref), https://doi.org/10.1007/s12020-012-9646-7.
Buffet, Alexandre. Identification de nouveaux gènes de prédisposition aux parangangliomes Positive impact of the knowledge of genetic status on the management and clinical outcome of patients with paraganglioma and/or pheochromocytoma Germline mutations in the mitochondrial 2-oxoglutarate/malate carrier SLC25A11 gene confer a predisposition to metastatic paragangliomas. Sorbonne Paris Cité, 25 septembre 2018. theses.fr, https://www.theses.fr/2018USPCB219.
Drouin, Jacques. « 60 YEARS OF POMC: Transcriptional and epigenetic regulation of POMC gene expression ». Journal of Molecular Endocrinology, vol. 56, no 4, mai 2016, p. T99‑112. DOI.org (Crossref), https://doi.org/10.1530/JME-15-0289.
Favier, Judith, et al. « Paraganglioma and Phaeochromocytoma: From Genetics to Personalized Medicine ». Nature Reviews Endocrinology, vol. 11, no 2, février 2015, p. 101‑11. DOI.org (Crossref), https://doi.org/10.1038/nrendo.2014.188.
Isidori, Andrea M., et al. « The Ectopic Adrenocorticotropin Syndrome: Clinical Features, Diagnosis, Management, and Long-Term Follow-Up ». The Journal of Clinical Endocrinology & Metabolism, vol. 91, no 2, février 2006, p. 371‑77. DOI.org (Crossref), https://doi.org/10.1210/jc.2005-1542.
Newell-Price, John, et al. « The CpG Island Promoter of the Human Proopiomelanocortin Gene Is Methylated in Nonexpressing Normal Tissue and Tumors and Represses Expression ». Molecular Endocrinology, vol. 15, no 2, février 2001, p. 338‑48. DOI.org (Crossref), https://doi.org/10.1210/mend.15.2.0599.
Picon, A., et al. « Analysis of Proopiomelanocortin Gene Transcription Mechanisms in Bronchial Tumour Cells ». Molecular and Cellular Endocrinology, vol. 147, no 1‑2, janvier 1999, p. 93‑102. DOI.org (Crossref), https://doi.org/10.1016/S0303-7207(98)00215-9.
Picon, A, et al. « Analysis of the Human Proopiomelanocortin Gene Promoter in a Small Cell Lung Carcinoma Cell Line Reveals an Unusual Role for E2F Transcription Factors ». Oncogene, vol. 18, no 16, avril 1999, p. 2627‑33. DOI.org (Crossref), https://doi.org/10.1038/sj.onc.1202635.
Ye, Lei, et al. « Hypomethylation in the promoter region of POMC gene correlates with ectopic overexpression in thymic carcinoids ». Journal of Endocrinology, vol. 185, no 2, mai 2005, p. 337‑43. DOI.org (Crossref), https://doi.org/10.1677/joe.1.05963.
